Химики часто относятся к энантиомерам, как к одному соединению, поскольку их химические свойства в обычных (ахиральных) условиях идентичны. Однако их биологическая активность может быть совершенно различной.
Это стало очевидным после трагической истории с талидомидом – лекарственным средством, которое в 60-е годы XX века врачи во многих странах прописывали беременным женщинам как эффективное снотворное и успокаивающее. Однако со временем проявилось его ужасное побочное действие: вещество оказалось тератогенным (повреждающим зародыш, от греческого teratos – чудовище, урод), и на свет появилась масса младенцев с врожденными уродствами.
Причины такого действия талидомида теперь хорошо изучены. Установлено, что этот препарат является смесью двух оптических изомеров, обладающих разной биохимической активностью:
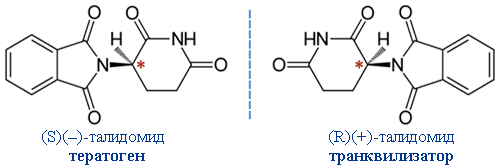
Один из изомеров – (R)(+)-талидомид – оказывает лечебное действие, другой – (S)(–)-талидомид –, напротив, является причиной тератогенного воздействия препарата, нарушая нормальный синтез белков. Вклиниваясь в клеточную ДНК, он препятствует нормальному процессу её транскрипции, необходимому для деления клеток и развития зародыша. Но тогда, в середине XX века, химики-фармацевты не слишком много знали о различной физиологической активности оптических изомеров, не умели их как следует разделять и не могли синтезировать один из энантиомеров в чистом виде.
Чем же объясняется различное действие энантиомеров? Человек – существо хиральное. Асимметрично и его тело, и молекулы биологически активных веществ, из которых оно состоит. Молекулы хиральных лекарств, взаимодействуя с определенными хиральными центрами организма, например, ферментами, могут действовать по-разному в зависимости от того, каким именно энантиомером является лекарство. «Правильное» лекарство подходит к своему рецептору, как ключ к замку и запускает желаемую биохимическую реакцию. Действие же «неправильного» антипода можно уподобить попытке пожать правой рукой правую же руку своего гостя.
В настоящее время многие лекарственные средства выпускаются в виде оптически чистых соединений. Так, из 25 наиболее распространенных с США лекарств только шесть являются нехиральными соединениями, три – это рацематы, остальные – чистые энантиомеры. Последние получают тремя методами:
- разделением рацемических смесей,
- модификацией природных оптически активных соединений (к ним относятся углеводы, аминокислоты, терпены, молочная и винная кислоты и др.),
- прямым синтезом.
Например, известная химическая фирма
Merck разработала способ производства гипотензивного препарата
метилдофа, включающий самопроизвольную кристаллизацию только нужного энантиомера путем введения в раствор небольшой затравки этого изомера. Прямой синтез также требует хиральных источников, поскольку любые другие традиционные методы синтеза дают оба энантиомера в равных пропорциях – рацемат. Это, кстати, одна из причин очень высокой стоимости некоторых лекарств, поскольку направленный синтез только одного из них – очень сложная задача. Поэтому не удивительно, что из более 500 синтетических хиральных препаратов, выпускаемых во всем мире, примерно лишь десятая часть являются оптически чистыми. В то же время из 517 препаратов, полученных из природного сырья, только восемь – это рацематы.
Необходимость в оптически чистых энантиомерах объясняется тем, часто только один из них обладает требуемым терапевтическим эффектом, тогда как второй антипод может вызвать нежелательные побочные эффекты или даже быть токсичным. Бывает и так, что каждый энантиомер обладает своим специфическим действием. Так, S(–)-
тироксин («левотроид») – это природный гормон щитовидной железы. А правовращающий R(+)-
тироксин («декстроид») понижает содержание холестерина в крови. Некоторые производители придумывают для подобных случаев торговые названия-палиндромы, например,
Darvon и
Novrad.
Если лекарство – рацемат, то один из энантиомеров может в лучшем случае оказаться индифферентным, в худшем – вызвать совершенно нежелательный эффект. Вот несколько примеров. Так, антиаритмическое средство S(–)-
анаприлин действует в 100 раз сильнее, чем
R(+)-форма! В случае
верапамила оба энантиомера обладают сходным эффектом, однако его
R(+)-форма обладает значительно менее сильным побочным кардиодепрессивным эффектом. Применяющийся для наркоза
кетамин может у 50% пациентов вызвать побочные эффекты в виде возбуждения, бреда и т.п., причем это присуще в основном только R(–)-изомеру, а также рацемату. У антигельминтного препарата
левамизола активен в основном в S(–)-изомер, тогда как его R(+)-антипод вызывает тошноту, поэтому в свое время рацемический левамизол был заменен одним из энантиомеров. Но, оказывается, экономически не всегда имеет смысл синтезировать чистые изомеры. Например, для широко применяющегося анальгетика
ибупрофена под действием ферментов возможна изомеризация терапевтически неактивной R(–)-формы в активный S(+)-изомер, поэтому в данном случае можно использовать значительно более дешевый рацемат.
Разное биологическое действие «правых» и «левых» изомеров проявляется не только среди лекарственных средств, а во всех случаях, когда хиральное соединение взаимодействует с живыми организмами. Яркий пример – аминокислота
изолейцин: ее правовращающий изомер сладкий, а левовращающий – горький. Другой пример.
Карвон – вещество с очень сильным ароматом (человеческий нос способен почувствовать его при содержании в воздухе всего 17 миллионных долей миллиграмма в литре). Карвон выделяют из тмина, в масле которого его содержится около 60%. Однако точно такое же соединение с тем же строением находится в масле кудрявой мяты – там его содержание достигает 70%. Каждый согласится с тем, что запах мяты и тмина вовсе не одинаковы. Оказалось, что на самом деле карвонов два – «правый» и «левый». Различие в запахе этих соединений показывает, что клетки-рецепторы в носу, ответственные за восприятие запаха, также должны быть хиральными.
Пеницилламин (3,3-диметилцистеин) – довольно простое производное аминокислоты цистеина. Это вещество применяют при острых и хронических отравлениях медью, ртутью, свинцом, другими тяжелыми металлами, так как оно обладает способностью давать прочные комплексы с ионами этих металлов; образующиеся комплексы удаляются почками. Применяют пеницилламин также при различных формах ревматоидного артрита, при системной склеродермии, в ряде других случаев. При этом применяют только S-форму препарата, так как R-изомер токсичен и может привести к слепоте.
Стереохимическая теория Вант-Гоффа далеко не сразу завоевала признание. Так, выдающийся немецкий химик-экспериментатор Адольф Кольбе, (его именем названо несколько органических реакций), опубликовал в мае 1877 года язвительную статью, в которой резко отрицательно отозвался о новой теории. К счастью, Кольбе оказался в явном меньшинстве, и теория Вант-Гоффа, заложившая основы современной стереохимии, завоевала общее признание, а ее создатель в 1901 стал первым лауреатом Нобелевской премии по химии.
Источник: Энциклопедия Кругосвет (http://www.krugosvet.ru/)
