Связь между структурой веществ и их биологической активностью
Выявление связи между химической структурой соединения и его физико-химическими свойствами, с одной стороны, и характеристиками биологической активности – с другой, позволяет предсказывать и прогнозировать последствия его попадания в организм, в биосферу и способствует целенаправленному синтезу веществ с заданными свойствами (исследования этого направления в фармакологии получили название драгдизайна – проектирования лекарств).
Говоря о связи структура-активность, следует иметь в виду, что структура означает строение вещества, определяющее все его физические и химические свойства; активность – это взаимодействие вещества с центрами-мишенями (места связывания) с наблюдаемым физиологическим эффектом.
Для анализа связи между структурой вещества и его биологической активностью используются различные физические и химические характеристики вещества. Параметры, изучаемые при установлении соотношения структура-активность: молекулярная масса вещества, плотность, молекулярный объем, критическое давление, коэффициент теплопроводности, теплоемкость, поверхностное натяжение, вязкость и др.
Как правило, биологическая активность ксенобиотика коррелирует с его способностью определенным образом распределяться между липидной и водной фазами.
Для оценки биологической активности ксенобиотика по его физико-химическим свойствам широко применяются методы, основанные на поиске корреляционных связей между этими показателями и биологической активностью. Для предсказания биологического эффекта неизвестного соединения следовало бы сравнивать структуру его молекулы и строение молекул всех важнейших веществ, обладающих заданной активностью (или токсичностью), но на практике к анализу привлекаются лишь некоторые основные вещества, обладающие характерным проявлением биологической активности.
Известно, что наиболее эффективные яды – это соединения, являющиеся аналогами природных биорегуляторов. Например, распространенный гербицид 2,4-Д (дихлорфеноксиуксусная кислота) близок в структурном отношении – по расположению карбоксильной группы относительно ароматического кольца – гормону индолилуксусной кислоте (ИУК), регулирующей ростовые процессы у растений. Попадая на листья, 2,4-Д легко поглощается и вызывает регуляторные расстройства, приводящие при высокой концентрации гербицида к гибели растения. Поскольку злаковые (вообще однодольные) оказались устойчивее к действию 2,4-Д, чем двудольные, его и стали применять для борьбы с сорняками.
В приведенной паре соединений структурное сходство очевидно: оба вещества – производные уксусной кислоты, содержащие ароматический заместитель. Не всегда, однако, способность соединения имитировать какой-то «естественный» метаболит обусловлена столь выраженным подобием молекулярного строения.
Другой пример – фосфорорганические инсектициды. Соединения этой группы «работают» под ацетилхолин, осуществляющий передачу импульса между двумя нервными клетками или нервной и мышечной клетками. Молекулы ацетилхолина (отработавшие) расщепляются ферментом холинэстеразой. Молекула холинэстеразы очень велика, она состоит из тысяч атомов, но в катаболическом акте наиболее важную роль играет определенная гидроксильная группа, к которой на мгновение присоединяется эфирная группа ацетилхолина. После завершения расщепления молекулы ацетилхолина продукты реакции отделяются от фермента.
Многие фосфорорганические соединения вида
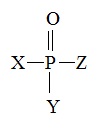
также способны взаимодействовать с гидроксилом, но они образуют с ним прочную, не поддающуюся расщеплению связь. Модифицированный таким образом фермент уже не может выполнять свою функцию – гидролиз ацетилхолина, что вызывает в конечном счете блокирование передачи нервных импульсов – паралич.
При исследовании закономерностей изменения биологической активности в ряду аналогов некоторого вещества модификации, вызывающие сдвиг биологической активности, обычно разделяют на две группы: модификации, связанные с изменением сродства молекулы к мембранактивным структурам (рецептору), и модификации, нарушающие развитие реакции системы на образование комплекса вещество-рецептор.
Сродство молекулы любого вещества к рецептору (активному центру) связано с определенными элементами ее пространственной структуры, обеспечивающими взаимную комплементарность рецептора и агониста. С другой стороны, внутренняя активность определяется преимущественно природой функциональных групп (присутствием в некоторых положениях ароматического радикала, кислотной группы, гидрофобной группы и т. п.).
Молекулы многих веществ имеют в растворе несколько стабильных конформаций, причем для осуществления акта взаимодействия с активным центром необходима лишь одна или немногие из них. Поэтому наряду с определением стабильных конформаций молекулы ксенобиотика возникает необходимость выявления биологически активной конформаций.
Под конформацией молекул следует понимать различные пространственные формы молекулы, возникающие при изменении относительной ориентации отдельных ее частей в результате внутреннего вращения атомов или групп атомов вокруг простых связей, изгиба связи и т. д.
Отметим некоторые показатели связи между структурой веществ и их биологической активностью:
– гидрофобность (липофилъность), определяемая соотношением в структуре молекулы гидрофобных и гидрофильных групп. Для организмов существенное значение имеет не столько сама гидрофобность, сколько сочетание двух свойств: гидрофобности и стабильности молекул в воде;
– ионизация (или другой показатель распределения электронов);
– содержание галогенов в молекуле ксенобиотика. Замена атомов водорода в молекуле вещества на атомы галогенов увеличивает устойчивость данного соединения;
– конформация молекул. Например, структура изадрина и его эпоксипроизводного эндрина легче атакуется ферментами, чем конформационно несколько иначе «вывернутая» структура альдрина и его эпоксидопроизводного – дильдрина. Этим, вероятно, можно объяснить то, что у млекопитающих эндрин метаболизируется быстрее, чем альдрин;
– замена двойной связи в молекуле на эпоксигруппу. Она приводит к увеличению биологической активности вещества и в ряде случаев повышает его персистентность.
