Основные реакции метаболизма ксенобиотиков
Ряд гидрофильных ксенобиотиков выводится из организма человека в неизменном виде, но большая их часть выделяется только после метаболических превращений. Основные тенденции метаболических процессов в организмах высших животных:
– снижение сложности молекулы;
– введение в молекулу при необходимости полярных заместителей;
– повышение растворимости ксенобиотика и/или его метаболита в воде посредством сопряжения (конъюгирования) еще до вывода из организма с последующей секрецией.
Общая картина превращения ксенобиотиков в высших организмах представляется следующей: 
Окислительные, восстановительные и гидролитические процессы называют функциональными или преконъюгационными реакциями, а процессы синтеза – конъюгационными.
Общей тенденцией является превращение экзогенного вещества в более полярную форму и последующее связывание образовавшегося производного с высокополярным фрагментом, который облегчает выделение ненужных организму веществ посредством имеющихся у него соответствующих функций.
Растения не имеют системы выделения, сравнимой с системой выделения животных, но их защитный механизм может включать связывание посторонних веществ некоторыми молекулами углеводов и накопление их в местах, лишенных метаболической активности, например, в вакуолях. Микроорганизмы способны разлагать многие сложные органические соединения на диоксид углерода и воду.
Реакции, участвующие в биотрансформации чужеродных веществ, как правило, разделяют на 4 класса: реакции окисления, восстановления, гидролиза и конъюгации.
Реакции окисления:
1) окисление спиртов и альдегидов;
2) окисление аминов. Например, реакция диэтиламина с нитритом в кислой среде желудка, в результате которой образуется канцероген – диэтилнитрозамин
Другой пример – реакция окисления симазина с образованием канцерогенного продукта:

Нитрит натрия ранее широко использовался в качестве консервирующей добавки к пищевым продуктам;
3) окисление ароматических аминов. Эти вещества подвергаются N-гидроксилированию, что может приводить к появлению канцерогенных продуктов:
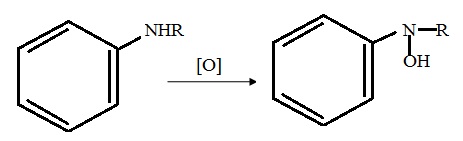
4) окисление ароматических алкилзамещенных соединений. Они обычно расщепляются между атомами C1 и С2 боковой цепи с образованием соответствующей ароматической кислоты:
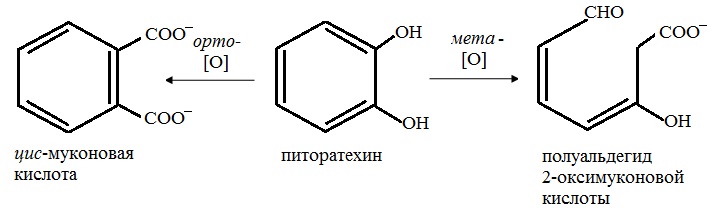
Эти реакции происходят с участием микроорганизмов, а также в растениях. У различных видов микроорганизмов удалось установить многочисленные реакции разрыва бензольного кольца. Обычно такие процессы весьма избирательны, поэтому универсальность почвенной экосистемы в превращениях различных классов соединений определяется разнообразием популяций микроорганизмов в почве;
5) гидроксилирование кольцевых систем. Алициклические кольцевые структуры гидроксилируются легче, чем ароматические. Это одна из причин высокой токсичности бензола, поскольку он тяжело окисляется до фенола. Большое значение имеет положение в ароматическом кольце неуглеродного заместителя.
Ароматическое гидроксилирование:
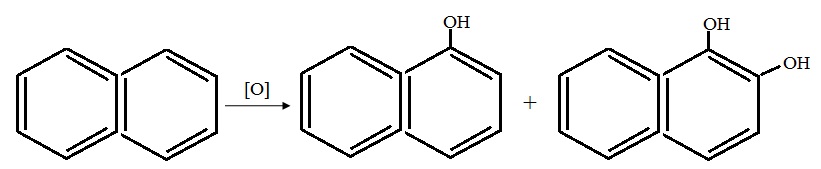
Алифатическое гидроксилирование: RCH3 → RCH2OH;
![]()
6) ароматизация алициклических соединений происходит в случае окисления циклогексанкарбоновых кислот с четным числом СН2-групп в боковой цепи) с участием митохондрий. Конечный продукт – бензойная кислота.
7) реакция эпоксидации. При реакциях окисления с участием фермента эпоксидазы образуется эпоксидное кольцо:
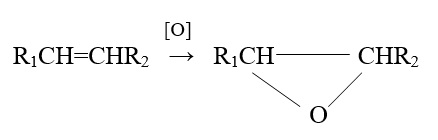
Эпоксиды высокотоксичны и обладают мутагенными и канцерогенными свойствами. Эпоксидации подвергаются многие ароматические соединения;
8) окисление или окислительное замещение органической серы. Гетероциклическая сера обычно окисляется в сульфоксиды или дисульфоны. Сера в алифатических комбинациях или ароматических боковых цепях иногда замещается кислородом. Например, инсектицид паратион (тиофос) метаболизируется микросомальными ферментами (а также в почве) в параоксон, который также обладает инсектицидными свойствами и почти вдвое более токсичен для млекопитающих, чем паратион:
(RO)3P=S → (RO)3P=O
паратион параоксон
(тиофос)
Превращение связи Р=S в связь Р=О приводит к повышению токсичности продуктов;
9) окислительное дезалкилирование О- и N-атомов. Эти реакции осуществляются оксигеназами микроорганизмов, а также клетками печени.
При окислительной биотрансформации ксенобиотиков нередко образуются более токсичные или канцерогенные соединения. Кроме отмеченных выше случаев, это может иметь место при окислении дибензантрацена в организме грызунов (образуются канцерогены) или при деградации некоторых азотсодержащих пестицидов, которые легко превращаются в высокомутагенные и канцерогенные соединения. Так, гербицид симазин окисляется в опасный канцероген.
Реакции восстановления:
1) восстановление некоторых альдегидов и кетонов в спирты под действием алкогольдегидрогеназ. Однако ацетон может прямо входить в цикл аэробного метаболизма через ацетоацетат и ацетил-КоА;
2) восстановление нитро- и азогрупп. Целый ряд ароматических нитросоединений, восстанавливаются в соответствующие амины нитроредуктазами:

Возможно образование продуктов, содержащих гидроксиамино- или нитрозогруппы (R-N=O). Образование нитрозосоединений представляет большую опасность для биосферы, так как при этом может образовываться вещество, обладающее сильным мутагенным и/или канцерогенным действием. Например, при биотрансформации гербицида трифлуралина происходит образование нитрозосоединения, обладающего канцерогенным действием;
3) восстановление N-оксидов. Процесс катализируется N-оксидо-редуктазами, которые обнаружены в микросомальной и растворимой фракциях клеток, а также в митохондриях;
4) восстановление дисульфидов (R–S–S–R1). Они расщепляются с образованием тиолов.
5) восстановление двойных связей. Двойные связи некоторых алифатических или алициклических соединений могут становиться насыщенными (например, у циклогексана). Простейшие алкены и алкины часто экскретируются без изменений их структуры;
6) дегидроксилирование;
7) восстановление ароматических циклов анаэробными микроорганизмами.
Реакции гидролиза:
1) гидролиз эфиров карбоновых кислот катализируют эстеразы. Эфиры карбоновых кислот гидролизуются в организме как животных, так и человека. Гидролиз эфирной связи – начальный этап микробиологической деградации многих пестицидов;
2) гидролиз амидов, гидразидов и нитрилов. Эти реакции происходят в дополнение к другим реакциям биотрансформации. Гидролиз амидной связи описан при изучении микробиологической деградации фениламидных пестицидов и происходит с участием амидаз:

3) гидролиз фосфорорганических веществ. В этом процессе участвуют ферменты, атакующие эфирные связи или действующие на ангидриды кислот. Реакция гидролиза эфира фосфорной кислоты проходит по следующей схеме:

Реакции конъюгации. К конъюгационным относятся процессы биосинтеза, в результате которых из ксенобиотиков или их метаболитов и эндогенных продуктов (глюкуроновой кислоты, ацетилсульфата, глицина и др.) образуются сложные вещества
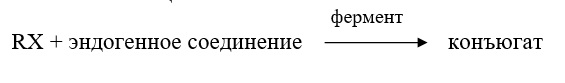
Образование конъюгатов – это энергозависимые процессы, подразделяющиеся на две группы в зависимости от природы активных промежуточных продуктов реакций:
– процессы, в результате которых образуются активированные конъюгирующие агенты: реакции метилирования, ацетилирования, образования глюкуронидов, гликозидов и сульфатов;
– процессы, для которых характерно образование активированного субстрата, например, аминокислотная конъюгация.
В определенных ситуациях реакции конъюгации считаются высокоэффективными путями снижения токсичности некоторых ксенобиотиков. Наиболее изучены следующие реакции конъюгации:
1) конъюгация ацетата при участии ацетил-КоА с некоторыми ароматическими аминами и сульфонамидами;
2) конъюгация глицина с бензойной кислотой, описанная Келлером в

3) конъюгация трипептида глутатиона. Глутатион – эффективный конъюгирующий агент для конденсирования кольцевых систем — нафталина, антрацена, фенантрена.
Глутатион принимает участие в реакциях биотрансформации таких устойчивых ксенобиотиков, как нафталин:

Многие ксенобиотики выделяются в мочу в виде меркаптуровых кислот. Такие конъюгаты образуются в результате взаимодействия ксенобиотиков с глутатионом;
1) метионин и этионин участвуют в реакциях алкилирования. Таким образом метилируется пиридин, пирогаллол; сульфиты, селениты, теллуриты подвергаются биологическому метилированию и превращаются в летучие диметильные производные;
2) орнитин используется при детоксикации бензойной кислоты в организме рептилий и птиц, а аргинин – в организмечленистоногих;
3) глутамин у приматов используется для конъюгации фенилуксусной кислоты и некоторых ее гетероциклических аналогов;
4) рибоза и глюкоза часто используются для конъюгации; конъюгаты глюкозы особенно широко представлены в растениях, у моллюсков и насекомых. Способность растений гликолизировать ксенобиотики была открыта в
8) конъюгация ксенобиотиков с глюкуроновой кислотой (образование глюкуронидов) – наиболее важный механизм детоксикации ксенобиотиков.
Глюкуроновая кислота используется для конъюгации с ксенобиотиками у большинства позвоночных и всех млекопитающих. Она имеет преимущество перед глюкозой как детоксицирующий агент, поскольку содержит ионизируемую группу. Конъюгации подвергаются спирты, фенолы, карбокислоты, амины, гидроксиламины, карбамиды, сульфонамиды и тиолы;
9) коньюгация с лигнином. С лигнином могут ковалентно связываться молекулы пестицидов 2,4-Д (дихлорфеноксиуксусная кислота), пентахлорфенола,а также 3,4-дихлоранилина;
10) сульфатная конъюгация (сульфатирование) – эволюционно один из древних видов биотрансформации. В нее вступаю фенолы, спирты, ароматические амины, гидроксиламины, некоторые стероиды. Происходит с участием сульфатаденилтрансферазы, аденилсульфаткиназы, и др. ферментов. В некоторых случаях сульфатная конъюгация приводит к появлению канцерогенного вещества, взаимодействующего с нуклеиновыми кислотами.
Описаны также и другие виды конъюгации (например, фосфатная конъюгация, реакция ксенобиотиков с глицинтаурином и формилом).
Дегалогенирование. К хлорсодержащим ксенобиотикам относятся многие персистентные поллютанты, в том числе пестициды, а также ряд природных метаболитов низших растений.
Можно выделить следующие виды реакций дегалогенирования:
1) гидролитическое дегалогенирование (хлорированных алифатических кислот, при деградации ароматических пестицидов).
2) восстановительное дегалогенирование − это реакция замещения атома галоида на водород.
3) Окислительное дегалогенирование. Реакции этого типа подразделяются на: дегидрогалогенирование (при метаболизме ДДТ); окислительное дегалогенирование с образованием двойной связи; дегалогенирование – гидроксилирование с участием молекулярного кислорода.
