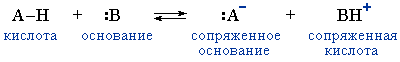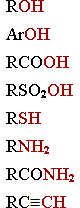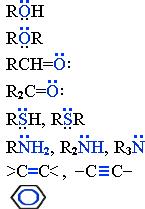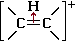Кислоты и основания Брёнстеда
Согласно протолитической теории Брёнстеда-Лоури, кислотность и основность веществ определяется переносом протона H
+.
Кислоты – соединения, способные отдавать протон (доноры H+).
Основания – cоединения, способные присоединять протон (акцепторы H+).
Кислота и основание образуют сопряженную кислотно-оснóвную пару. Кислотные свойства проявляются в присутствии основания, оснóвные – в присутствии кислоты.
Кислотно-оснóвное равновесие отражается схемой:
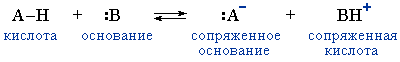
Кислотами и основаниями могут быть как нейтральные молекулы различных классов органических соединений, так и ионы.
| Кислоты – доноры H+ |
Основания – акцепторы H+ |
| Класс соединений |
Формула |
Класс соединений |
Формула |
| Нейтральные молекулы |
Нейтральные молекулы |
Спирты
Фенолы
Карбоновые кислоты
Cульфоновые кислоты
Тиолы
Амины
Амиды
Алкины-1 |
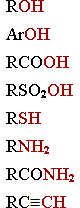 |
Спирты
Простые эфиры
Альдегиды
Кетоны
Тиолы, тиоэфиры
Амины
Алкены, алкины
Арены |
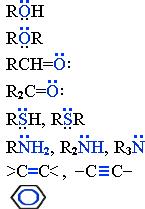
|
| Катионы |
Анионы |
Алкилоксоний
Алкиламмоний
σ-Комплекс
Карбокатион |
R–OH2+
R–NH3+

R2C+–CH3
|
Гидроксид-ион
Алкоксид-ион
Алкилсульфид-ион
Амид-ион
Ацилат-ион
Карбанион
Гидрид-ион |
OH¯
RO¯
RS¯
H2N¯
RCOO¯
R3C¯
H¯
|
- Носителем протона является кислотный центр молекулы кислоты – атом водорода, связанный с электроотрицательным элементом (O, S, N, реже С), т.е. полярная связь: элементδ-←Нδ+.
- Акцептором протона служит оснóвный центр молекулы основания – атом с неподелённой парой электронов (n-основание), либо π-электроны локализованной или делокализованной кратной связи (π-основание).
По типу кислотного центра органические кислоты классифицируют как OH-, SH-, NH- и СН-кислоты. По характеру оснóвного центра
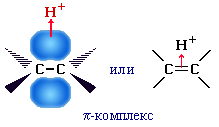
n-основания подразделяются на N-, O- и S-основания. К π-основаниям относятся алкены, алкины и арены, которые за счёт π-электронной пары образуют с протоном не ковалентные связи, а короткоживущие π-комплексы (интермедиаты). Например:
Кислоты Брёнстеда
| Название |
Формула |
pKa |
Сопряженное
основание |
| ОН-кислоты |
Муравьиная
Уксусная
Бензойная
Фенол
Метанол
Этанол |
HCOOH
CH3COOH
C6H5COOH
C6H5OH
CH3OH
C2H5OH |
3,75
4,76
4,19
10,0
15,5
16,0 |
HCOO¯
CH3COO¯
C6H5COO¯
C6H5O¯
CH3O¯
CH3CH2O¯ |
| SН-кислоты |
Этантиол
Тиофенол |
CH3SH
C6H5SH |
10,5
6,5 |
CH3S¯
C6H5S¯ |
| NН-кислоты |
Аммиак
Ацетамид
Диацетиламид |
NH3
CH3CONH2
(CH3CO)2NH |
33
15,1 |
NH2¯
CH3CONH¯
(CH3CO)2N¯ |
| СН-кислоты |
Ацетилен
Хлороформ
Нитрометан
Диметилмалонат
Дицианометан |
HC≡CH
CHCl3
CH3NO2
CH2(COOCH3)2
(CN2)2CH2 |
25
15,7
10,6
15,7
11,1 |
HC≡C:¯
¯:CCl3
¯:CH2NO2
¯:CH(COOCH3)2
¯:CH(CN)2 |
|
Основания Брёнстеда
Название |
Формула |
Сопряженная
кислота |
pKBH+ |
| N-основания |
Аммиак
Метиламин
Этиламин
Диэтиламин
Триметиламин
Анилин |
NH3
CH3NH2
C2H5NH2
(C2H5)2NH
(CH3)3N
C6H5NH2 |
NH4+
CH3NH3+
C2H5NH3+
(C2H5)2NH2+
(CH3)3NH+
C6H5NH3+ |
9,25
10,6
10,7
10,9
9,8
4,6 |
| O-основания |
Вода
Метанол
Фенол
Диэтил. эфир
Ацетон
Мочевина |
H2O
CH3OH
C6H5OH
(C2H5)2O
(CH3)2С=O
(NH2)2С=O |
H3O+
CH3OH2+
C6H5OH2+
(C2H5)2OH+
(CH3)2С=OH+
(NH2)2С=OH+ |
-1,7
-2
-6
-5
-7
0,1 |
| S-основания |
Этантиол
Диэтилсульфид |
C2H5SH
(C2H5)2S
|
C2H5SH2+
(C2H5)2SH+ |
-7
|
| π-основания |
Этилен |
H2C=CH2 |
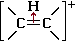 |
|
|
Кислотно-оснóвные свойства соединений зависят от их строения.
- Сила кислоты определяется стабильностью сопряженного основания (аниона), образующегося при отщеплении протона. Чем стабильнее анион, тем сильнее кислота.
- Сила основания зависит как от доступности пары электронов в оснóвном центре, так и от стабильности образующегося катиона (сопряженной кислоты). Более стабильному катиону соответствует более сильное основание.
- Между кислотой и основанием сопряженной пары существует взаимосвязь: чем сильнее кислота, тем слабее сопряженное основание и, наоборот – сильному основанию соответствует слабая сопряженная кислота.
В целом кислотность и основность определяется совокупностью ряда факторов:
- электроотрицательность и поляризуемость атомов,
- степень делокализации зарядов в ионах,
- способность ионов к сольватации, т.е. взаимодействию с молекулами растворителя.
Сила кислот Брёнстеда возрастает c увеличением электроотрицательности атомов, связанных с атомом водорода:
CH-кислота < NH-кислота < OH-кислота < SH-кислота.
В той же последовательности увеличивается стабильность соответствующих анионов, образующихся при отщеплении протона. Электроноакцепторные заместители повышают устойчивость анионов за счёт делокализации отрицательного заряда, а электронодонорные заместители, напротив, уменьшают её.
Основность (способность присоединять протон)
n-оснований с одинаковыми заместителями при гетероатоме снижается в ряду:
R-NH2 > R-OH > R-SH ("правило" NOS)
Этот порядок определяется электроотрицательностью и поляризуемостью гетероатома в центре основности. Среди элементов второго периода (O и N) более электроотрицательный кислород прочнее удерживает неподелённую электронную пару по сравнению с азотом (т.е. амины более сильные основания, чем спирты). В случае серы (элемент третьего периода), обладающей более высокой поляризуемостью, электронная плотность неподелённой пары электронов рассредоточена в бóльшем объёме. Поэтому атом серы слабее связывает протон. Следовательно, тиолы наиболее слабые основания. Стабильность ониевых катионов (аммониевых, оксониевых, сульфониевых) уменьшается в том же порядке (см.
значения pK
BH+ сопряженных кислот). При этом электронодонорные заместители стабилизируют катионы, а электроноакцепторные – дестабилизируют.