Глоссарий
Требуемые условия завершения
Изомерия органических соединений
Обзор глоссария по алфавиту
Специальные | А | Б | В | Г | Д | Е | Ё | Ж | З | И | К | Л | М | Н | О | П | Р | С | Т | У | Ф | Х | Ц | Ч | Ш | Щ | Э | Ю | Я | Все
Д |
|---|
И |
|---|
Изомерия – явление существования соединений, имеющих одинаковый состав, но различное строение и, следовательно, разные свойства. Соединения одинакового состава (с одинаковой молекулярной формулой), отличающиеся строением, называются изомерами. | |
О |
|---|
Оптическая активность– способность вещества вращать плоскость луча поляризованного света. | |
П |
|---|
Плоскость симметрии– (зеркальная плоскость) представляет собой воображаемую плоскость, которая проходит через молекулу и делит ее на две зеркально равные части, то есть одна часть молекулы является точным зеркальным отражением другой. | |
Поляриметр– прибор для измерения угла оптического вращения плоскости луча поляризованного света. Подробнее >> | |
Правила Кана-Ингольда-Прелога– правила определения старшинства заместителей при установлении R,S-конфигурации энантиомеров и Z,E-конфигурации диастереомеров. Основаны на сравнении атомных номеров элементов в Периодической системе. Старшинство заместителей возрастает с увеличением номера атома, связанного с асимметрическим центром. Неподелённая пара электронов считается заместителем, имеющим атомный номер 0. Если атомы "первого слоя" одинаковы, старшинство определяют по атомам "второго слоя". При тождественности атомов "второго слоя" рассматриваются атомы "третьего слоя" и т.д. Атом, связанный двойной связью, учитывается дважды, а тройной связью – трижды. В случае изотопно различимых заместителей старшим считается изотоп с большим массовым числом. | |
Проекции Фишера– графическое изображение проекции тетраэдрической модели молекулы, ориентированной так, чтобы две связи располагались по вертикали и были направлены назад от наблюдателя, а две другие связи располагались по горизонтали и были направлены вперед – к наблюдателю (т.е. связи тетраэдрического атома ориентированы под углом 90°). Например: 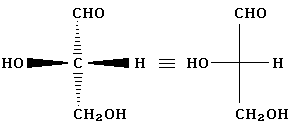 | |
Р |
|---|
Радиус Ван-дер-ВаальсаВан-дер-ваальсов радиус характеризует "размер" данного атома по отношению к другим атомам, с которыми он не связан химическими связями. Это минимальное расстояние на которое могут сблизится несвязанные атомы. Ван-дер-ваальсовыми радиусами считают половину межъядерного расстояния между ближайшими одноимёнными атомами, не связанными между собой химической связью. При сближении атомов на расстояние, меньшее суммы их ван-дер-ваальсовых радиусов, возникает сильное межатомное отталкивание. Поэтому ван-дер-ваальсовы радиусы характеризуют минимальные допустимые контакты атомов, принадлежащих разным молекулам. | |
Радиус ковалентныйКовалентный радиус соответствует половине длины ковалентной связи между двумя одинаковыми атомами. | |
Рацемат– смесь равных количеств энантиомеров. Рацемат не обладает оптической активностью, обозначается знаком (±). | ||
